Примеры решения задач
Задача 1. Каким образом можно осуществить реакции: ацетат натрия → уксусная кислота → хлоруксусная кислота? Напишите уравнения реакций.
Решение. Уксусная кислота — слабая, поэтому сильные кислоты вытесняют ее из ее солей: CH3COONa + HCl = СН3СООН + NaCl.
Уксусная кислота на свету реагирует с хлором:
СН3СООН + Сl2 = СН2СlСООН + HCl↑.
Задача 2. Как можно получить пропионовую кислоту из бромэтана?
Решение. СН3СН2Br → СН3СН2СООН.
В молекуле пропионовой кислоты содержится три атома углерода, а в молекуле бромэтана — два. Дополнительный атом углерода можно ввести в состав молекулы, используя реакцию замещения с цианидом калия:
CH3CH2Br + KCN → CH3CH2CN + КBr.
В этой реакции образуется нитрил пропионовой кислоты (этилцианид), который гидролизуется при нагревании с образованием пропионата аммония:
CH3CH2CN + 2Н2О → СН3СН2СООМН4.
Подкисление раствора пропионата аммония дает пропионовую кислоту:
CH3CH2COONH4 + HCl → СН3СН2СООН + NH4Cl.
Другой способ решения этой задачи связан с использованием магнийорганических соединений и может быть проиллюстрирован схемой:
Мg СО2. Н2О
С2Н5Br → С2Н5МgBr → С2Н5СООМgBr → С2Н5СООН
Задача 3. Напишите схему превращений, с помощью которой из 3,3,3-трихлорпропена можно получить 3-гидроксипропановую кислоту. Укажите условия проведения реакций.
Решение. Хлороводород присоединяется к 3,3,3-трихлорпропену против правила Марковникова за счет -/-эффекта группы ССl3:
ССl3-СН=СН2 + HCl →ССl3-СН2-СН2Сl.
Гидролиз образующегося тетрахлорпроизводного водным раствором КОН дает (после подкисления) гидроксикислоту:
CCl3CH2CH2Cl + 4KOH → НООС-СН2-СН2ОН + 4KCl + Н2О
Задача 4. Уксусную кислоту массой 5,40 г поместили в сосуд объемом 4,50 л и нагрели до температуры 200 °С. Давление паров при этом составило 43,7 кПа. Определите число молекул димера уксусной кислоты в газовой фазе.
Решение. В парах уксусная кислота находится частично в виде димеров, а частично в виде отдельных молекул:
х моль х/2 моль
2СН3СООН → (СН3СООН)2
Исходное количество уксусной кислоты: v(CH3COOH) = m/ M = 5,4 / 60 = 0,09 моль. Пусть в реакцию димеризации вступило х моль СН3СООН, тогда образовалось х/2 моль димера (СН3СООН)2 и осталось (0,09 — х) моль СН3СООН. Общее количество веществ в газовой фазе равно:
v = PV / (RT) = 43,7 * 4,50 / (8,31 * 473) = 0,05 = х/2 + (0,09 – х),
откуда х = 0,08 моль. Число молекул димера уксусной кислоты в газовой фазе равно:
N[(СН3СООН)2] = v * NA = 0,08 / 2 * 6,02*1023 = 2,408*1022.
Ответ. 2,408*1022 молекул (СН3СООН)2.
Задача 5. Напишите уравнения реакций, соответствующие следующей схеме:
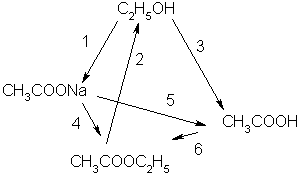
Решение.
1) Этанол окисляется до ацетата натрия хроматом натрия в щелочном растворе:
ЗС2Н5ОН + 4Na2CrO4 + 7NaOH + 4H2O = 3CH3COONa + 4Na3[Cr(OH)6].
2) Этилацетат гидролизуется под действием щелочей:
СН3СООС2Н5 + NaOH = CH3COONa + С2Н5ОН.
3) Этанол окисляется до уксусной кислоты дихроматом калия в кислом растворе:
5С2Н5ОН + 4KMnO4 + 6H2SO4 = 5СН3СООН + 2K2SO4 +4MnSO4 + 11H2O.
4) Этилацетат можно получить из ацетата натрия действием этилиодида:
CH3COONa + C2H5I = СН3СООС2Н5 + Nal.
5) Уксусная кислота — слабая, поэтому сильные кислоты вытесняют ее из ацетатов:
CH3COONa + HCl = СН3СООН + NaCl
6) Сложный эфир образуется при нагревании уксусной кислоты с этанолом в присутствии серной кислоты:
| H2SO4 | ||
| СН3СООН + С2Н5ОН |
|
СН3СООС2Н5 + Н2О |
