Получение алюминия
Впервые металлический алюминий был получен химическим путем немецким химиком Ф.Велером в 1821 г. (восстановлением из хлорида алюминия металлическим калием при нагревании).
В 1854 г. французский ученый Сент-Клер Девиль предложил электрохимический способ получения алюминия, восстанавливая натрием двойной хлорид алюминия-натрия. По способу Сент-Клер Девиля с 1855 по 1890 г. было получено всего 200 тонн алюминия, а за оставшиеся до конца XIX века 10 лет выплавка алюминия (уже по новому способу) составила 28000 тонн, в 1930 г. мировое производство алюминия только в нашей стране составило несколько млн. тонн в год.
Новый способ был предложен в 1886 г. американским химиком Ч. Холлом — он заключается в электролизе Аl2O3, растворенного в расплавленном криолите Nа3АlF6, — и применяется до настоящего времени.
Основным сырьем при получении алюминия являются бокситы (гидратированный оксид алюминия Аl2О3.xН2О, «загрязненный», как правило, оксидами SiO2, Fе2О3, СаСО3): нефелины (КNа3[АSiO4]4 или 3/2[Nа2О.Аl2О3.2SiO2].1/2[К2О.Аl2О3.2SiO2]); алуниты (КАl(SО4)2.2Аl(ОН)3); каолины (Аl2[(Si2О5)(ОН)4]) и глиноземы (смесь каолинов с песком SiO2, известняком CaCO3, магнезитом МgСО3).
В промышленности алюминий получают электролизом раствора чистого Аl2О3 в расплавленном криолите NaАlF6 с добавкой СаF2 при температуре ~950 °С. Криолит используется как растворитель оксида алюминия, кроме того, с добавкой СаF2 он позволяет поддерживать в электролитической ванне температуру плавления не выше 1000°.
Первым этапом в переработке руд является их очистка от примесей, вторым этапом — тщательное обезвоживание оксида алюминия.
Электролиз водных растворов соединений алюминия невозможен, так как ион Аl3+ более активен, чем ион Н3О+, и на катоде из водных растворов соединений алюминия будет выделяться водород.
Электролиз проводят в стальных электролитических ваннах, у которых имеется внешняя теплоизоляция и внутренняя футеровка из огнеупорного кирпича 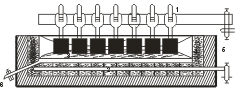 . Внутри электролитическая ванна выложена графитовыми блоками, так как расплавленные фториды при высокой температуре растворяют обычную огнеупорную футеровку. Графитовые блоки у основания ванны вместе с расплавленным алюминием служат катодом, а аноды представляют собой угольные стержни, которые смонтированы таким образом, чтобы они могли опускаться по мере их сгорания (окисление анодов происходит с образованием СО и СО2).
. Внутри электролитическая ванна выложена графитовыми блоками, так как расплавленные фториды при высокой температуре растворяют обычную огнеупорную футеровку. Графитовые блоки у основания ванны вместе с расплавленным алюминием служат катодом, а аноды представляют собой угольные стержни, которые смонтированы таким образом, чтобы они могли опускаться по мере их сгорания (окисление анодов происходит с образованием СО и СО2).
В первую очередь в электролизер загружают криолит и фторид кальция. После их расплавления (теплом, которое выделяется при пропускании электрического тока) добавляют чистый Аl2О3.
Выделяющийся на аноде кислород окисляет угольные стержни, именно поэтому конструкция электролитической ванны такова, что аноды можно опускать по мере их сгорания. В результате каждые 20-30 дней аноды приходится заменять новыми.
В этом процессе потребляется большое количество электрической энергии. В нем используется постоянный ток силой более 100000 А при напряжении порядка 5 В. Для получения 1 т алюминия расходуется 13-17 тысяч киловатт-часов энергии. Такой процесс экономически оправдан только при наличии дешевой электроэнергии, например, от гидростанции. В России для этого имеются все условия, особенно в Сибири, на базе дешевой электроэнергии и больших запасов нефелиновых руд.
