Неорганическая химия

Вода — наиболее распространенное соединение на Земле. Ее количество достигает 1018 т, и она покрывает приблизительно четыре пятых земной поверхности. Это единственное химическое соединение, которое в природных условиях существует в виде жидкости, твердого вещества (лед) и газа (пары воды). Вода играет жизненно важную роль в промышленности, быту и в лабораторной практике; она совершенно необходима для поддержания жизни. Приблизительно две трети человеческого тела приходятся на долю воды, и многие пищевые продукты состоят преимущественно из воды. Содержание воды в некоторых пищевых продуктах Пищевые продукты Содержание воды, масс. % Помидоры Грибы Молоко Апельсины Яблоки Рыба Картофель Яйца Мясо (говядина) 95 92 87 86 84 82 76 75 64…
Оксид углерода (II) и оксид кремния (II)
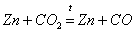
Оба оксида получают неполным окислением простых веществ или по реакциям: С + СО2 = 2СО, Si + SiO2 = 2SiO. Они оба не реагируют при обычных условиях ни с кислотами, ни со щелочами. Оксид кремния (II) мало доступен и очень редко используется, в отличие от угарного газа СО, на свойствах которого мы остановимся ниже. Оксид…
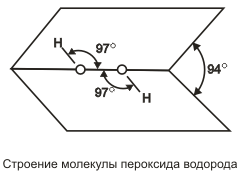
Пероксид водорода (перекись водорода) Н2О2 — тяжелая полярная жидкость голубоватого цвета, строение которой показано на . В жидком состоянии молекулы пероксида водорода сильно ассоциированы благодаря водородным связям. Поскольку пероксид водорода имеет больше возможностей к образованию таких связей (ввиду большего числа атомов кислорода на один атом водорода), чем вода, то он имеет большие плотность, вязкость и температуру кипения (150,2°С). Пероксид водорода смешивается с водой во всех отношениях, чистый Н2О2 и весьма концентрированные растворы взрываются на свету; 30%-ный раствор пероксида водорода в воде имеет техническое название «пергидроль». Пероксид водорода каталитически разлагается при комнатной температуре, выделяя в первый момент атомарный кислород. На этом основано использование 3%-ного раствора Н2О2 в медицине. Пероксид водорода вступает в реакции трех типов: без изменения пероксидной группировки: Ва(ОН)2 + Н2О2 = ВаО2 + 2Н2О, в качестве восстановителя: 2KMnО4 + 5Н2О2 + ЗН2SО4 = 2MnSО4 + К2SО4 + 5О2 + 8Н2O,…
Оксид углерода (IV), Угольная кислота и ее соли
Оксид углерода (IV) (диоксид углерода, углекислый газ) — газ без цвета и запаха, не поддерживающий дыхания и горения, тяжелее воздуха. Он растворим в воде (88 объемов СО2 в 100 объемах Н2О при 20°С). При обычных давлениях твердый диоксид углерода переходит в газообразное состояние (сублимируется), минуя жидкое состояние. При обычной температуре под давлением 60 атм переходит…
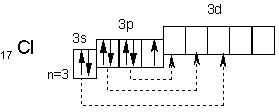
В подгруппу галогенов входят фтор, хлор, бром, иод и астат (астат — радиоактивный элемент, изучен мало). Это р—элементы VII группы периодической системы Д.И. Менделеева. На внешнем энергетическом уровне их атомы имеют по 7 электронов ns2np5. Этим объясняется общность их свойств. Свойства элементов подгруппы галогенов Свойства F Cl Br I At 1. Порядковый номер 9 17 35 53 85 2. Валентные электроны 2s22p5 3s23p5 4s24p5 5s25p5 6s26p5 3. Энергия ионизации атома, эВ 17,42 12,97 11,84 10,45 9,2 4. Относительная электроотрицательность 4,1 2,83…
Оксид кремния (IV) и кремниевые кислоты
Оксид кремния SiO2 — твердое, очень тугоплавкое вещество (температура плавления более 1700 °С), широко распространенное в природе, где оно встречается главным образом в виде минерала кварца, а также кристобалита и тридимита. При обычных температурах устойчивой модификацией является кварц, с ростом температуры наблюдаются полиморфные превращения: Кремнезем всех модификаций в виде мономера не существует; он всегда полимерен…
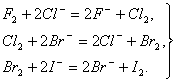
Все галогены проявляют высокую окислительную активность, которая уменьшается при переходе от фтора к йоду. Фтор — самый активный из галогенов, реагирует со всеми металлами без исключения, многие из них в атмосфере фтора самовоспламеняются, выделяя большое количество теплоты, например: 2Аl + 3F2 = 2АlF3 + 2989 кДж, 2Fе + 3F2 = 2FеF3 + 1974 кДж. Без нагревания фтор реагирует и со многими неметаллами (H2, S, С, Si, Р) — все реакции при этом сильно экзотермические, например: Н2 + F2 = 2НF + 547 кДж, Si + 2F2 = SiF4(г) + 1615 кДж. При нагревании фтор окисляет все другие галогены по схеме Hal2 + F2 = 2НаlF где Наl = Сl, Вr,…
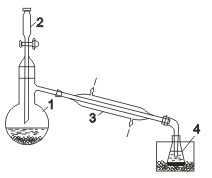
Промышленное получение фтора и хлора связано с электролитическими процессами. Ввиду высокой окислительной активности фтора его получают исключительно электролизом расплавов фторидов металлов (в том числе и в лабораториях); хлор получают электролизом как расплавов, так и растворов хлоридов. Бром и йод получают химическим способом. При электролизе расплава хлорида натрия (Тпл = 801°С) на катоде выделяется металлический натрий, а на аноде — газообразный хлор. Электролитическая ванна (электролизер) представляет собой футерованный огнеупорным кирпичом стальной сосуд. В качестве анода используют графитовые стержни, в качестве катода — стальной цилиндр. В верхней части ванны имеется устройство для сбора хлора (колокол). Выделяющийся в катодном пространстве металлический натрий собирают в коллектор (устройство для сбора натрия без доступа воздуха). Таким образом, электролиз расплава NaCl — способ одновременного получения хлора и металлического натрия. Электролизом водного раствора NаСl получают одновременно Н2, Сl2 и гидроксид натрия NаОН. Обычно электролизу подвергают насыщенный водный раствор NaCl (рассол), подаваемый в электролизер сверху. Электролиз протекает по следующей схеме: NaCl Na+ + Сl— Н2О Н+ + ОН— ↓ ↓ ↓ (-) Катод (+) Анод 2Н+ + 2е =…

Галогеноводороды, галогеноводородные кислоты и галогениды. Все галогеноводороды при обычных условиях газообразны. Химическая связь, осуществляемая в их молекулах, — ковалентная полярная, причем полярность связи в ряду НF — НСl — НВr — НI падает. Прочность связи также уменьшается в этом ряду. Вследствие своей полярности, все галогеноводороды, в отличие от галогенов, хорошо растворимы в воде. Так, при комнатной температуре в 1 объеме воды можно растворить 400 объемов НСl, 530 объемов НВr и около 400 HI. Свойства галогеноводородов Галогено-водород Температура плавления оС Температура кипения оС Энергия связи кДж/моль Константа диссоциации кислоты НF —80 20 562 6,7∙10—4 НСl -115 -85 431 1.107 НВr -89 -67 366…
Кислород — второй по электроотрицательности элемент после фтора, поэтому он проявляет сильные окислительные свойства. С большинством металлов он реагирует уже при комнатной температуре, образуя основные оксиды. С неметаллами (за исключением гелия, неона, аргона) кислород реагирует, как правило, при нагревании. Так, с фосфором он реагирует при температуре ~ 60 °С, образуя Р2О5, с серой — при температуре около 250 °С: S + О2 = SO2. С графитом кислород реагирует при 700 °С С + О2 = СО2. Взаимодействие кислорода с азотом начинается лишь при 1200°С или в электрическом разряде N2 + О2 2NО — Q. Кислород реагирует и со многими сложными соединениями, например с оксидом азота (II) он реагирует уже при комнатной температуре: 2NО + О2…
