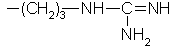Общая характеристика.
Многие биологически активные молекулы включают несколько химически различных функциональных групп, способных к взаимодействию между собой или с функциональными группами других молекул. Один из примеров — моносахариды, в состав которых входят несколько гидроксильных групп и одна карбонильная группа. Другой важный пример бифункциональных природных соединений — аминокислоты.
Аминокислоты — это органические бифункциональные соединения, в состав которых входят карбоксильная группа -СООН и аминогруппа -NН2. В зависимости от взаимного расположения обеих функциональных групп различают α-, β-, γ-аминокислоты:
β α β α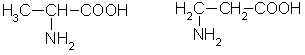
α-аминопропионовая β-аминопропионовая
кислота кислота
Греческая буква при атоме углерода обозначает его удаленность от карбоксильной группы. Здесь будут рассматриваться только α-аминокислоты, поскольку другие аминокислоты в природе не встречаются.
В состав белков входят 19 основных аминокислот и одна иминокислота. Все природные аминокислоты имеют тривиальные названия.
Иминокислота пролин (молекулярная формула C5H9NO2) имеет структуру
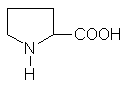
Простейшая аминокислота — глицин (аминоуксусная кислота). Остальные природные аминокислоты можно разделить на следующие основные группы:
α-Аминокислоты общей формулы
![]()
| Аминокислота |
Обозначение (трёх- и одно- буквенное) |
—R |
Молеку-лярная формула |
| Глицин |
Gly(G) |
-H |
C2H5NO2 |
|
Аланин |
Ala(A) |
-CH3 |
C3H7NO2 |
|
Валил |
Val(V) |
-CH(CH3)2 |
C5H11NO2 |
|
Лейцин |
Leu(L) |
-CH2-CH(CH3)2 |
C6H13NO2 |
|
Изолейцин |
Ile(I) |
-CH2-CH(CH3)-C2H5 |
C7H15NO2 |
|
Цистеин |
Cys(C) |
-CH2-SH |
C3H7SNO2 |
|
Метионин |
Met(M) |
-CH2-CH2-S-CH3 |
C5H11SNO2 |
|
Серин |
Ser(S) |
-CH2-OH |
C3H7NO3 |
|
Треонин |
Thr(t) |
-CH(OH)-CH3 |
C4H9NO3 |
|
Фенилаланин |
Phe(F) |
-CH2-C6H5 |
C9H11NO2 |
|
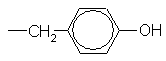
Тирозин |
Tyr(Y) |
|
C9H11NO3 |
|
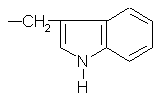
Триптофан |
Trp(W) |
|
C11H12N2O2 |
|
Аспарагиновая кислота |
Asp(D) |
—CH2COOH |
C4H7NO4 |
|
Глутаминовая кислота |
Glu(E) |
-CH2-CH2-COOH |
C5H9NO4 |
|
Аспарагин |
Asn(N) |
-CH2-CO-NH2 |
C4H8N2O3 |
|
Глутамин |
Gln(Q) |
-CH2-CH2-CO-NH2 |
C5H10N2O3 |
|
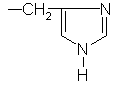
Гистидин |
His(H) |
|
C6H9N3O2 |
|
Лизин |
Lys(K) |
-(CH2)4-NH2 |
C6H14N2O2 |
|
Аргинин |
Arg(R) |
|
C6H14N4O2 |
1) гомологи глицина — аланин, валин, лейцин, изолейцин;
2) серосодержащие аминокислоты — цистеин, метионин;
3) аминокислоты с алифатической гидроксильной группой — серин, треонин;
4) ароматические аминокислоты — фенилаланин, тирозин, триптофан;
5) аминокислоты с кислотным радикалом — аспарагиновая и глутаминовая кислоты;
6) аминокислоты с амидной группой — аспарагин, глутамин;
7) аминокислоты с основным радикалом — гистидин, лизин, аргинин.