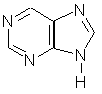
Пурин — гетероцикл, включающий два сочлененных цикла: пиримидиновый и имидазольный. Ароматическая система пурина включает 10 p-электронов (8 электронов двойных связей и два неподеленных электрона пиррольного атома азота). Пурин — амфотерное соединение. Слабые основные свойства пурина связаны с атомами азота шестичленного цикла, а слабые кислотные свойства — с группой NH пятичленного цикла. Основное значение пурина состоит…
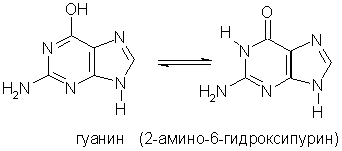
Пуриновые основания — производные пурина, остатки которых входят в состав нуклеиновых кислот: аденин, гуанин.

Пластмассами называют материалы на основе полимеров, способные изменять свою форму при нагревании и сохранять новую форму после охлаждения. Благодаря этому свойству пластмассы легко поддаются механической обработке и используются для производства изделий с заданной формой. Пластмассы бывают двух основных типов: термопластичные и термореактивные. Термопластичные пластмассы могут многократно изменять свою форму при нагревании и последующем охлаждении. К…
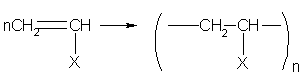
Полиэтилен (-СН2-СН2-)n — один из простейших полимеров. Его молекулярная масса колеблется от 20 тыс. до 3 млн. в зависимости от способа получения. Полиэтилен с низкой молекулярной массой и разветвленной структурой получают радикальной полимеризацией этилена при высоком давлении (120-150 МПа) в присутствии кислорода или органических пероксидов. Если процесс полимеризации проходит при низком давлении в присутствии металлоорганических…
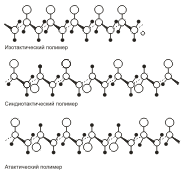
Полипропилен (-СН2-СН(СН3)-)n получают полимеризацией пропилена под давлением в присутствии металлоорганических катализаторов. При этом образуется стереорегулярный полимер. Полипропилен по свойствам похож на полиэтилен, однако отличается от него более высокой температурой размягчения (160-170 °С против 100-130 °С). Полипропилен используют для изготовления изоляции, труб, деталей машин, химической аппаратуры, канатов. Конфигурации полимеров на основе монозамещенных производных этилена. Большие кружки…

Полистирол (-СН2-СН(С6Н5)-)n — термопластичный полимер, имеющий линейную структуру и молекулярную массу от 50 тыс. до 300 тыс. По свойствам он похож на полиэтилен. Температура размягчения атактического полистирола 85 °С, а изотактического полимера — 230 °С. Полистирол используют для изготовления деталей радиоаппаратуры, облицовочных плит, посуды, игрушек и других изделий. Широко применяются сополимеры стирола с акрилонитрилом и…

Поливинилхлорид (-CH2—CHCl-)n — термопластичный полимер с молекулярной массой от 300 до 400 тыс. Он отличается хорошей прочностью и высокой химической стойкостью, поэтому из него изготавливают детали химической аппаратуры, работающей в агрессивных средах.
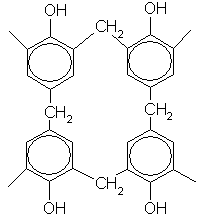
Фенолоформальдегидная смола — термореактивный полимер, который получают по реакции поликонденсации фенола с формальдегидом в присутствии кислот. Начало процесса поликонденсации можно представить следующим образом: Образующаяся молекула может через молекулу формальдегида соединяться с другими молекулами фенола. Если процесс соединения происходит только в орото-положениях к ОН-группе, то образуется линейный термопластичный полимер. При нагревании этого полимера возможно соединение различных…
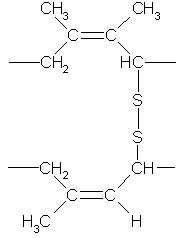
Каучуки — продукты полимеризации диенов и их производных. Натуральный каучук получают из латекса — сока некоторых тропических растений. Его строение можно установить по химическим свойствам: каучук присоединяет бром, бромоводород и водород, а при нагревании без доступа воздуха распадается с образованием изопрена (2-метилбутадиена). Это означает, что каучук представляет собой непредельный полимер — полиизопрен. При более детальном…
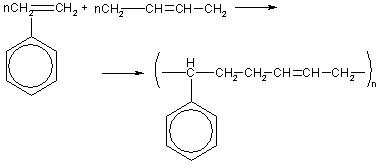
Промышленный спрос на каучук значительно превосходит возможности его природных источников, поэтому химикам пришлось решать проблему синтеза каучука, не уступающего по свойствам натуральному продукту. Первый промышленный синтетический каучук был получен в России в 1931 г. Профессор С.В.Лебедев открыл экономичный способ производства бутадиена из этилового спирта и осуществил полимеризацию бутадиена по радикальному механизму в присутствии металлического натрия:…
