Получение и свойства этена
Соберем простой прибор. Для этого понадобятся две пробирки. К одной из них подберем пробку с двумя отверстиями и вставим в нее изогнутую стеклянную трубку и термометр со шкалой до 250 °С. Все соединения должны быть достаточно плотными, чтобы образующийся газ мог выходить только через трубку.
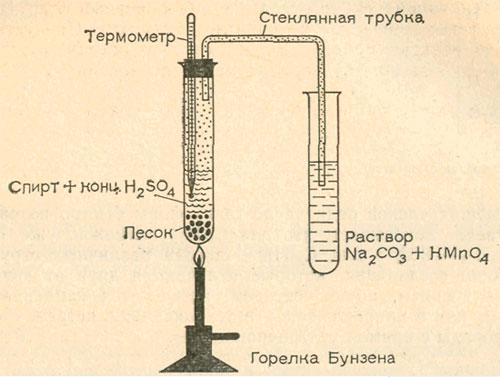
В пробирку поместим 2 мл денатурированного спирта и осторожно, малыми порциями, добавим 5 мл концентрированной серной кислоты (только в защитных очках!). При этом смесь очень сильно разогреется, и мы сразу же почувствуем приятный запах — это выделяется этен, пока в малом количестве. Можно добавить в пробирку еще 1—2 г мелкого чистого песка, чтобы ускорить реакцию. Однако можно этого и не делать.
Во вторую пробирку нальем 5—10 мл 10%-ного раствора соды (карбоната натрия) и добавим несколько капель раствора перманганата калия. Раствор должен получиться интенсивно фиолетовым, но не слишком тёмным. Он называется реактивом Байера.
Теперь соберем прибор и будем нагревать первую пробирку горелкой Бунзена до тех пор, пока термометр, погруженный в смесь спирта с серной кислотой, не покажет 150— 170 °С.
По стеклянной трубке отводится газообразный этен (теперь мы легко узнаем его по приятному запаху). Пропустим его через реактив Байера. Вскоре раствор обесцветится и одновременно выделятся коричневые хлопья оксида марганца (IV).
Если найдется немного бромной воды, можно разбавить ее водой в соотношении 1:1 и через полученную бурую жидкость пропустить этен. (Осторожно! Пары брома действуют на глаза и дыхательные пути). Окраска бромной воды исчезнет. После этого можно поджечь этен, все еще выделяющийся из изогнутой стеклянной трубки. Он горит светящимся, слегка коптящим пламенем.
Ненасыщенные углеводороды, в противоположность насыщенным, легко вступают в химические реакции. Так, в нашем опыте этен окислялся кислородом из перманганата калия, а перманганат калия при этом восстанавливался. Так же, как правило, ведут себя по отношению к реактиву Байера и другие ненасыщенные углеводороды. Реакционная способность этих веществ объясняется тем, что их двойные или тройные связи расщепляются с образованием простых связей. При этом за счет свободных валентностей присоединяются атомы или группы атомов, например кислород или бром.
CH2 = CH2 + 1/2O2 + H2O → HO – CH2 – CH2 – OH
CH2 = CH2 + Br2 → Br – CH2 – CH2 -Br
Применение этена и этина (ацетилена) в промышленности обусловлено тем, что, в отличие от алканов, они обладают высокой реакционной способностью. Именно благодаря ей на основе этена и этина можно построить множество различных органических соединений.
Источник: Э.Гроссе, Х.Вайсмантель, «Химия для любознательных»
