Не всякий лёд из воды
Тот, кто после напряженной работы или длительной прогулки по пыльной улице отведает лимонаду или газированной воды, ощутит освежающее действие этих напитков. Любителям газированных напитков необходим сифон, знаток восхваляет устойчивую пену пива, весело играет шампанское в бокалах на праздничном столе.
Крошечные пузырьки газа разрыхляют тесто, благодаря им булочки становятся мягкими. Во всех случаях здесь действует один и тот же углекислый газ (диоксид углерода). Тысячи кубических метров этого газа ежедневно выбрасываются из дымовых труб. В природном круговороте веществ он играет решающую роль, на нем основаны многие химические процессы, а в твердом виде он представляет собой чрезвычайно распространенное охлаждающее средство — сухой лед.
С помощью нескольких опытов мы можем познакомиться важнейшими свойствами диоксида углерода, который является ангидридом угольной кислоты:
H2O + CO2 → H2CO3
Известно, что многие кислоты образуются в результате взаимодействия оксидов неметаллов с водой. Ангидриды — это химические соединения, которые возникают из других соединений при отделении воды, и, наоборот, переходят в исходные соединения при поглощении воды. Угольная кислота в чистом виде не существует. Равновесие изображенной выше реакции сильно сдвинуто в сторону исходных продуктов. Угольная кислота диссоциирует в две стадии и образует сначала гидрокарбонат, затем карбонат-ионы:

Соответствующие соли называются гидрокарбонаты и карбонаты. Сложим оба равенства, в результате получим:
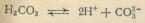
Если записать равновесие диссоциации в виде закона действия масс, то константа диссоциации будет иметь вид:
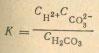
причем ее точное значение при 25 °С составит 2,4 * 10-16 моль2/л2. Из этого следует, что угольная кислота относится к слабым электролитам, то есть к таким, чья константа диссоциации меньше 10-4 моль2/л2.
Источник: Э.Гроссе, Х.Вайсмантель, «Химия для любознательных»
