Практическая химия

После того как мы рассмотрели природные хлориды и сульфаты в качестве основного сырья для химического производства, необходимо сказать немного о силикатах. Кремний — второй по распространенности (после кислорода) элемент в литосфере нашей планеты (почти 28%). Он встречается преимущественно в виде кремнекислых солей различных металлов, а также в форме чистого оксида (кварц SiO2). Анионы силикатов могут…
Получение кислорода простыми способами

Укрепим пробирку из тугоплавкого стекла на штативе и внесем в нее 5 г порошкообразной селитры (нитрата калия КNО3 или нитрата натрия NaNO3). Поставим под пробирку чашку из огнеупорного материала, наполненную песком, так как при этом опыте стекло часто плавится и вытекает горячая масса. Поэтому и горелку при нагревании будем держать сбоку. Когда мы сильно нагреем…

Заполним хлором несколько больших пробирок, для этого подведем в них сверху газ, используя опущенную на дно сосуда трубку. Хлор в 2,5 раза тяжелее воздуха, поэтому он полностью вытеснит последний из пробирки. В первую пробирку поместим зеленые листочки и цветы разной окраски, в другую — несколько полосок голубой и красной лакмусовой бумаги, несколько цветных лоскутков материи,…
Выделение кремневой кислоты из жидкого стекла

Имеющееся в продаже жидкое стекло представляет собой сиропообразный раствор силиката натрия (Na2Si2O3)n или калия (K2Si2O3)n. В смеси с различными добавками, такими как глинозем, гипс или опилки его можно использовать для изготовления замазок. Оно находит широкое применение при получении огнеупорной краски и огнеупорных покрытий. В пробирку с разбавленным наполовину жидким стеклом будем добавлять по капле соляную…

Применим собранный кислород для опытов по окислению. Внесем в наполненные кислородом пробирки небольшие, по возможности тонкоизмельченные, пробы свинца, меди, алюминия, цинка и олова и неплотно закроем пробирки ватой. При нагревании металлы сгорят с появлением яркого пламени; в пробирках останутся оксиды. В чистом кислороде сгорит также тонкая железная проволока. Придадим ей спиралеобразную форму и укрепим на…
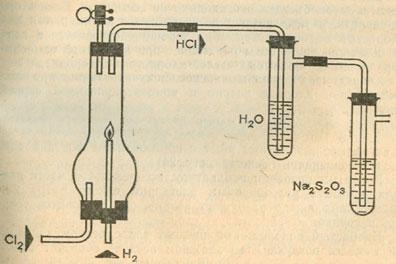
Для синтеза нам нужны два аппарата для получения газов. В одном будем получать водород из разбавленной серной кислоты и цинка, а в другом — хлор из соляной кислоты и перманганата калия. Пропустив оба газа через концентрированную серную кислоту, высушим их и затем, сжигая водород в атмосфере хлора, получим хлористый водород. Закроем ламповое стекло или широкий…
Цемент с наполнителем дает бетон

Бетон сейчас, несомненно, является важнейшим строительным материалом. Покрытия автострад, плиты, столбы, балки, конструкции современных жилых домов и промышленных построек выполнены большей частью из бетона. Бетонные смеси различаются плотностью, прочностью и теплоизоляционными свойствами. Объединяет их то, что они все состоят из цемента и через некоторое время после смешивания с водой затвердевают, поглощая влагу. В этом заключается…

В природе кислород встречается в виде двухатомных молекул. Атомарный кислород О обладает чрезвычайно сильной окислительной способностью. Он получается при разложении озона, молекула которого содержит три атома кислорода: О3 → О2 + О Если на налитую в фарфоровую чашку концентрированную серную кислоту насыпать немного тонкораспыленного перманганата калия, образуется озон. (Надеть защитные очки! Взрывоопасно!) Будем держать над…

Еще в давние времена были известны стекло и мыло. Для их изготовления применяли карбонат натрия (соду), который добывали на берегах содовых озер в Африке и Америке или получали из золы морских и прибрежных растений на побережьях Европы. Примерно 150 лет назад соду стали производить химико-технологическим методом. Первый процесс изготовления соды разработал француз Леблан. Но с…
Лёйна задохнулась бы без азота

Если бы в начале нашего века учитель географии в немецкой гимназии спросил своего ученика о Лёйне, то он едва ли получил бы удовлетворительный ответ. В то время Лёйна была деревней а государственном округе Мерзебург и насчитывала около трехсот жителей. В географической книге 1899 г. говорится, что там расположены залежи бурого угля, который может быть использован…
