Горение веществ (Часть 4)
Взрыв газовых смесей с воздухом
В стакан объемом 100 — 150 мл наливают 20 — 50 мл раствора шампуни (можно взять любой стиральный порошок или мыло). С помощью резиновой груши или интенсивным перемешиванием добиваются образования небольшого количества пены в стакане. Затем через раствор в стакане пропускают горючий газ (водород, метан, этилен, ацетилен) до заполнения стакана пузырями моющего средства и убирают газоотводную трубку. Горящей лучинкой поджигают смесь газов в стакане. Происходит вспышка.
Самовоспламенение белого фосфора
В сухую пробирку кладут на дно небольшой комочек сухого красного фосфора, вставляют стеклянную палочку и нагревают в узком пламени горелки, стараясь нагреть только фосфор. Красный фосфор превращается в белый, который конденсируется в виде маслянистых капель на конце палочки у дна пробирки. Если теперь вынуть палочку из пробирки (берегитесь ожога!), то фосфор воспламеняется и сгорает ярким пламенем, выделяя обильный дым оксида.
«Извержение вулкана»
На асбестовую сетку или металлический лист (можно взять и фарфоровую чашечку), укрепленные на штативе, насыпают дихромат аммония и нагревают пламенем горелки. Через несколько минут начинается экзотермическая реакция с выделением азота, паров воды и обильного «пепла» — оксида хрома (III). Процесс сопровождается выбросом искр и эффектно имитирует извержение вулкана.
Опыт можно разнообразить соответствующей декорацией. Особенно эффектно протекает «извержение», если внутри кучки дихромата аммония поместить несколько шариков роданида ртути (II), которые при разложении создают имитацию выхода лавы на поверхность вулкана.
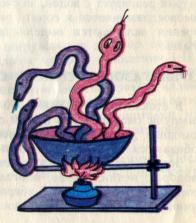 «Фараоновы змеи»
«Фараоновы змеи»
Если небольшие шарики (величиной с фасоль) роданистой ртути поместить в фарфоровую чашку и нагреть, то газообразные продукты реакции, вспучивая получаемую золу, образуют выпячивания в виде ползущих змей. Этот опыт, придуманный египетскими жрецами для устрашения молящихся, получил название «фараоновы змеи».
Роданид ртути можно получить из нитрата ртути (II) и роданида калия или аммония. Для этого 7 г нитрата ртути (II) растворяют в 50 мл воды и подкисляют несколькими каплями азотной кислоты. Отдельно готовят раствор роданида калия (4 г соли на 20 мл воды) или роданида аммония (3 г соли на 20 мл воды). Оба раствора сливают, выпавший осадок роданида ртути отфильтровывают (лучше на воронке Бюхнера под вакуумом) и подсушивают. Из слегка влажной массы формуют (в резиновых перчатках) небольшие шарики диаметром до 1 см и оставляют сушить на воздухе. Высушенный препарат следует хранить в плотно закрытых баночках. При отсутствии нитрата ртути (II), его можно получить либо из ртути, либо из оксида ртути (II) взаимодействием с азотной кислотой.
Для получения соли из ртути нагревают (под тягой!) до 50 — 60°С 100 мл 30%-ной азотной кислоты, добавляют в нее порциями 20 г металлической ртути до полного растворения (осторожно, выделяется диоксид азота!). Для определения полноты окисления ртути делают пробу с соляной кислотой (в 0,5 мл реакционной смеси добавляют 2 — 3 капли соляной кислоты, отсутствие появления мути указывает на полноту окисления металла), Если муть появляется, то добавляют еще 5 — 10 мл азотной кислоты, стараясь избежать избытка кислоты. В полученном растворе содержится около 33 г нитрата ртути.
Полученный раствор делят на четыре равные части и используют для синтеза роданида ртути (II), как указано выше. Для получения нитрата ртути (II) из оксида отвешивают 11 г оксида ртути (II) и растворяют в небольшом избытке азотной кислоты (около 40 мл 30%-ного раствора). Полученный раствор содержит около 15 г нитрата ртути (II), его делят на две части и используют для синтеза роданистой ртути (II), как указано выше.
Примечание. Получение всех препаратов осуществляет только учитель и обязательно под тягой.
«Химия на досуге», Г.И. Штремплер
- Реакции лекарственных веществ и препаратов бытовой химии (Часть 4)
- Реакции лекарственных веществ и препаратов бытовой химии (Часть 3)
- Реакции лекарственных веществ и препаратов бытовой химии (Часть 2)
- Реакции лекарственных веществ и препаратов бытовой химии (Часть 1)
- Окраска веществ (Часть 2)
- Окраска веществ (Часть 1)
- Горение веществ (Часть 6)
- Горение веществ (Часть 5)
- Горение веществ (Часть 3)
- Горение веществ (Часть 2)
